VI
Medical
MEDICAL 4 - marzo 2014
Nella sua attuale configurazione il Twinstream
Mult Mode Respirator ha due ventilatori che fun-
zionano indipendentemente l’uno dall’altro a di-
versa frequenza e con diverse pressioni. Il primo
serve a fornire i 12 respiri al minuto convenzionali
mentre il secondo è più potente e può erogare cir-
ca 800 respiri in un minuto. In pratica, la seconda
ventilazione ad alta frequenza è più efficiente nel
muovere l’aria dentro e fuori i polmoni e serve a
ridurre lo stress su questi delicati organi durante le
operazioni più lunghe che possono richiedere molte ore
di ventilazione forzata e questo perché rimuove l’anidri-
de carbonica più facilmente e fa in modo che l’ossigeno
raggiunga i polmoni più in profondità e sia assorbito più
efficacemente nel circolo sanguigno.
La gestione dei rischi
La correlazione fra i rischi e i benefici sui pazienti dev’es-
sere sempre la migliore possibile allo stato attuale della
tecnologia. Ciò significa che per ogni prodotto medicale
dev’essere fatta un’attenta valutazione dei rischi seguendo
la procedura schematizzata in figura come consigliano gli
esperti Escatec.
In pratica, una completa valutazione dei rischi deve con-
siderare tutti i rischi ossia, innanzi tutto, sui pazienti, ma
poi anche per gli utilizzatori delle apparecchiature, per le
terze parti e anche sull’ambiente. Invero, i rischi possono
sempre comparire sia durante il quotidiano
funzionamento degli strumenti sia nei tempi
di attesa, durante l’immagazzinaggio o an-
che per danni accidentali e tutte queste pro-
babilità di rischio devono essere considerate
e documentate se si vuole davvero prevenire
i guai che potrebbero risultare da tali rischi.
La stima della probabilità di danneggiamen-
to e della gravità degli eventuali danni per
ciascun singolo rischio può essere fatta solo
dopo un’approfondita analisi e solo seguen-
do una corretta e attenta classificazione si
può decidere se i rischi sono giustificabili
o ingiustificati e di conseguenza scegliere
le misure precauzionali adeguate. Secondo
gli esperti Escatec i seguenti principi devo-
no essere applicati esattamente nell’ordine
esposto: innanzi tutto eliminare o minimiz-
zare i rischi per la sicurezza delle persone;
in secondo luogo prendere le dovute pre-
cauzioni (compresi i sistemi di allarme) per
i rischi che non possono essere eliminati;
infine, informare gli utenti circa i rischi re-
sidui per i quali non ci sono appropriate o
adeguate precauzioni (con opportuni ma-
nuali istruzioni oppure corsi di formazione e
addestramento). Se le misure correttive applicate sono effi-
caci allora il rischio scende e può essere valutato come giu-
stificabile, ma se è ancora troppo alto occorre nuovamente
e ripetutamente intervenire con adeguamenti che possano
mitigarlo fino a renderlo davvero giustificabile. Non si può
completare un ciclo di valutazione per un prodotto medi-
cale finché tutti i rischi e tutte le probabilità di rischio non
raggiungono la classificazione “giustificabile” e questo ci-
clo di test è fondamentale e imprescindibile durante ogni
fase di industrializzazione per qualsiasi nuovo MP.
Requisiti severi
Il principale standard che riguarda lo sviluppo e la realiz-
zazione dei prodotti medicali in Europa è la Linea Guida
Europea 93/42 EWG. I requisiti base sono descritti nell’ap-
pendice 1 di questa linea guida alla quale tutti i costruttori
e i distributori devono fare riferimento. Ciò significa che
tutti devono rispettare le normative standard
e le direttive attuative ivi descritte sia per le
caratteristiche che riguardano genericamen-
te tutti i prodotti sia per le specifiche stret-
tamente legate a ciascun prodotto perché
personalizzate a funzionalità specifiche.
Per la verità non è mai obbligatorio seguire
tutte le norme, ma è certamente consiglia-
bile.
Un costruttore deve dimostrare sufficiente
sicurezza sui suoi prodotti sia per il rispet-
to degli standard esistenti sia nell’adegua-
mento delle caratteristiche all’attuale stato
dell’arte della tecnologia. In alcuni casi,
eventualmente, può essere comprensibile
fare eccezioni sulle singole norme se queste
non sono state aggiornate sulle nuove tecno-
logie, ma solo se si tratta di innovazioni adot-
tate da tutti i costruttori come risultato della
ricerca e sviluppo svolta in laboratorio e in
grado di offrire prestazioni manifestamente
migliori rispetto allo standard.
I singoli paragrafi dell’appendice 1 della li-
nea guida possono essere analizzati e valutati
solo con una lunga e approfondita esperien-
za sul campo.
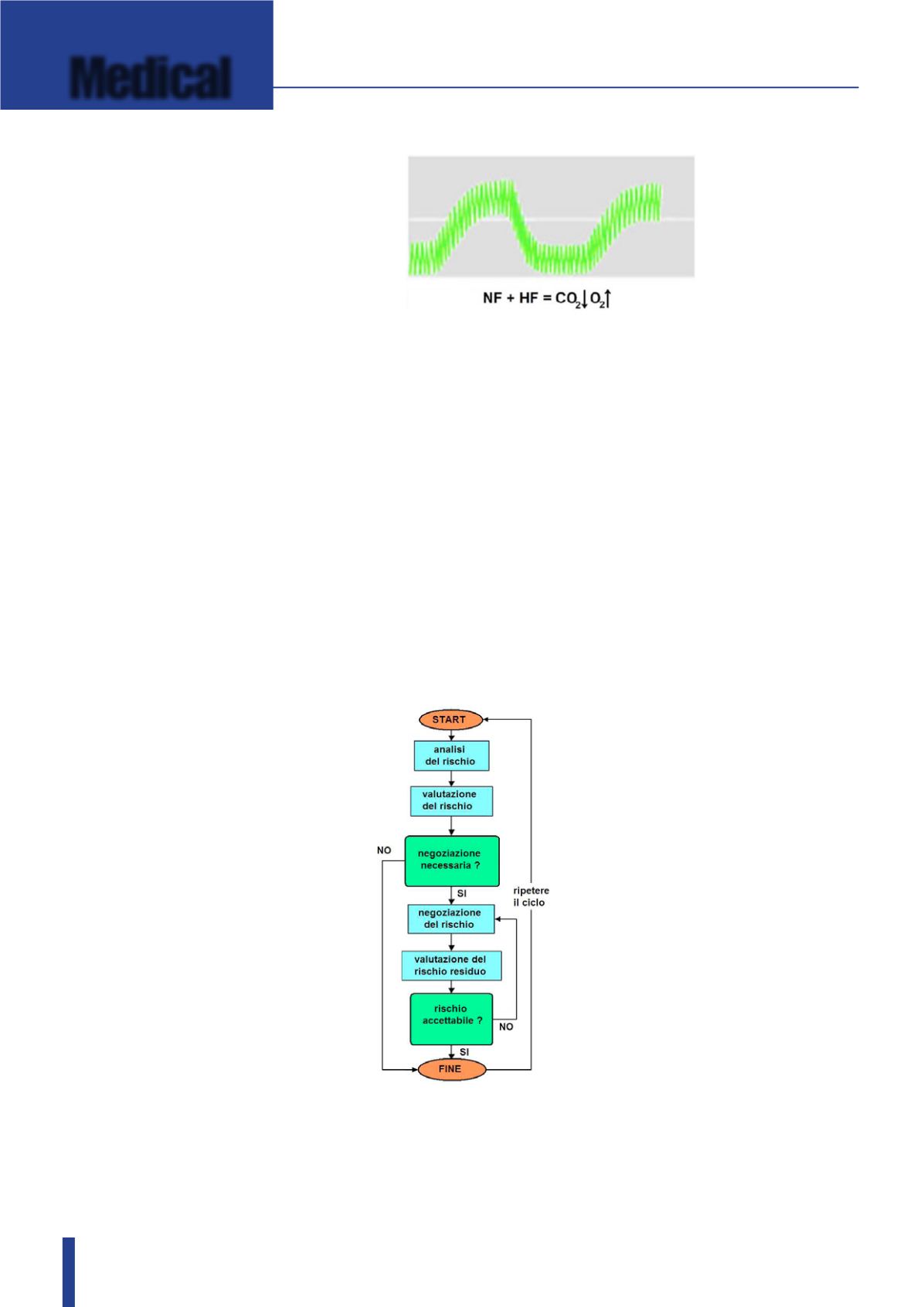
Fig. 2 – Reazione chi-
mica alla base del prin-
cipio di funzionamento
del Twinstream di cui
Escatec ha curato lo
sviluppo
Fig. 3 – L’algoritmo ciclico per
l’analisi del rischio sui prodot-
ti medicali consigliato dagli
esperti Escatec


